![]()
![]() Dosimetría comparativa del anticuerpo
monoclonal radiomarcado ¹³¹I-ChiTn en tumores pulmonares murinos tratados con
losartán
Dosimetría comparativa del anticuerpo
monoclonal radiomarcado ¹³¹I-ChiTn en tumores pulmonares murinos tratados con
losartán
 Comparative isotropy of the ¹³¹I-ChiTn
radiolabeled monoclonal antibody in murine lung tumors treated with losartan
Comparative isotropy of the ¹³¹I-ChiTn
radiolabeled monoclonal antibody in murine lung tumors treated with losartan
Análise comparativa da isometria do anticorpo monoclonal radiomarcado com ¹³¹I-ChiTn em tumores pulmonares murinos tratados com losartan
![]()
https://doi.org/10.35954/SM2026.45.1.2.e301
Marcos Tassano a https://orcid.org/0000-0001-6685-4656
Pablo Cabral b https://orcid.org/0000-0001-7344-2027
(a) Universidad de la República, Facultad de Ciencias, Centro de Investigaciones Nucleares, Área de Radiofarmacia, Laboratorio de Radioquímica. Montevideo, Uruguay.
(b) Universidad de la República, Facultad de Ciencias. Profesor Agregado de Radiofarmacia. Montevideo, Uruguay.
Cómo citar este artículo / Citation this article / Como citar este artigo
Tassano M, Cabral P. Dosimetría comparativa del anticuerpo monoclonal radiomarcado ¹³¹I-ChiTn en tumores pulmonares murinos tratados con losartán. Salud Mil [Internet]. 18 de marzo de 2026 [citado DD de MM de AAAA]; 45(1):e301. Disponible en: https://revistasaludmilitar.uy/ojs/index.php/Rsm/article/view/476 DOI: 10.35954/SM2026.45.1.2.e301.
RESUMEN
Introducción: la radioinmunoterapia permite administrar radiación ionizante de forma selectiva a células tumorales mediante anticuerpos monoclonales radiomarcados. El anticuerpo quimérico anti-Tn (ChiTn) radiomarcado con ¹³¹I constituye una estrategia potencial para el tratamiento dirigido de tumores que expresan este antígeno.
Objetivo: estimar el efecto del pretratamiento con losartán sobre la distribución de dosis absorbida de ¹³¹I-ChiTn en un modelo murino de tumor pulmonar Tn+.
Metodología: la dosis absorbida fue estimada mediante integración de curvas tiempo-actividad derivadas de datos de biodistribución previamente publicados y aplicación del formalismo MIRD para dosimetría interna.
Resultados: aumento de la captación tumoral del radiofármaco en presencia de losartán, con incremento de la dosis absorbida tumoral de 1.5 a 1.8 mGy/MBq en tumores Tn+, sin incrementos relevantes en la dosis a órganos críticos.
Discusión: estos resultados sugieren que la modulación farmacológica del microambiente tumoral mediante losartán podría mejorar el índice terapéutico de la radioinmunoterapia con ¹³¹I-ChiTn y optimizar la eficacia terapéutica de este radioanticuerpo.
PALABRAS CLAVE: Anticuerpos Monoclonales; Dosimetría; Microambiente Tumoral; Radioinmunoterapia; ¹³¹I-ChiTn.
ABSTRACT
Introduction: Radioimmunotherapy allows for the selective delivery of ionizing radiation to tumor cells using radiolabeled monoclonal antibodies. The anti-Tn chimeric antibody (ChiTn) radiolabeled with ¹³¹I represents a potential strategy for the targeted treatment of tumors that express this antigen.
Objective: To estimate the effect of pretreatment with losartan on the absorbed dose distribution of ¹³¹I-ChiTn in a murine model of Tn+ lung tumor.
Methodology: The absorbed dose was estimated by integrating time-activity curves derived from previously published biodistribution data and applying the MIRD formalism for internal dosimetry.
Results: Increased tumor uptake of the radiopharmaceutical in the presence of losartan, with an increase in the tumor absorbed dose from 1.5 to 1.8 mGy/MBq in Tn+ tumors, without significant increases in the dose to critical organs.
Discussion: These results suggest that pharmacological modulation of the tumor microenvironment using losartan could improve the therapeutic index of radioimmunotherapy with ¹³¹I-ChiTn and optimize the therapeutic efficacy of this radiolabeled antibody.
KEYWORDS: Antibodies, Monoclonal; Dosimetry; Tumor Microenvironment; Radioimmunotherapy; ¹³¹I-ChiTn.
RESUMO
Introdução: A radioimunoterapia permite administrar radiação ionizante de forma seletiva às células tumorais por meio de anticorpos monoclonais radiomarcados. O anticorpo quimérico anti-Tn (ChiTn) radiomarcado com ¹³¹I constitui uma estratégia potencial para o tratamento direcionado de tumores que expressam esse antígeno.
Objetivo: Estimar o efeito do pré-tratamento com losartan sobre a distribuição da dose absorvida de ¹³¹I-ChiTn em um modelo murino de tumor pulmonar Tn+.
Metodologia: A dose absorvida foi estimada por meio da integração de curvas tempo-atividade derivadas de dados de biodistribuição previamente publicados e da aplicação do formalismo MIRD para dosimetria interna.
Resultados: Aumento da captação tumoral do radiofármaco na presença de losartan, com aumento da dose absorvida tumoral de 1,5 para 1,8 mGy/MBq em tumores Tn+, sem aumentos relevantes na dose em órgãos críticos.
Discussão: Esses resultados sugerem que a modulação farmacológica do microambiente tumoral por meio do losartan poderia melhorar o índice terapêutico da radioimunoterapia com ¹³¹I-ChiTn e otimizar a eficácia terapêutica desse radioanticorpo.
PALAVRAS-CHAVE: Anticorpos Monoclonais; Dosimetria; Microambiente Tumoral; Radioinmunoterapia; ¹³¹I-ChiTn.
INTRODUCCIÓN
La radioinmunoterapia constituye una estrategia terapéutica dirigida que combina la especificidad molecular de los anticuerpos monoclonales con el efecto citotóxico de la radiación ionizante administrada mediante radionucleidos terapéuticos (1).
El radionucleido ¹³¹I presenta características particularmente favorables para este propósito, incluyendo emisión beta terapéutica, emisión gamma útil para imagen y una vida media física de aproximadamente ocho días (2).
Sin embargo, la eficacia de los radioanticuerpos en tumores sólidos suele verse limitada por factores propios del microambiente tumoral, como presión intersticial elevada, fibrosis estromal y arquitectura vascular desorganizada, que restringen la penetración homogénea del anticuerpo en el tejido tumoral (3,4).
Se ha demostrado que la inhibición del sistema renina-angiotensina puede mejorar la perfusión tumoral y facilitar la penetración de agentes terapéuticos al reducir la presión intersticial tumoral (5).
El antígeno Tn constituye una glicoproteína truncada sobreexpresada en múltiples carcinomas humanos, incluyendo pulmón, mama y colon (6).
El desarrollo de anticuerpos monoclonales dirigidos contra este antígeno ha permitido explorar nuevas estrategias de radioinmunoterapia dirigidas a tumores sólidos (7).
En estudios preclínicos recientes se ha demostrado que el anticuerpo quimérico anti-Tn radiomarcado puede presentar captación tumoral significativa en modelos murinos de cáncer pulmonar (8).
El objetivo de este trabajo fue realizar un análisis dosimétrico traslacional del radioanticuerpo ¹³¹I-ChiTn en tumores pulmonares murinos Tn+ y evaluar el impacto del pretratamiento con losartán sobre la captación tumoral y la dosis absorbida.
MATERIALES Y MÉTODOS
Datos
Los datos experimentales de biodistribución (%ID/g) en tumor y órganos (hígado, riñón, estómago y tiroides) a 4, 24 y 48 horas (h) postinyección fueron extraídos de una investigación de autores uruguayos (8), utilizando los datos abiertos disponibles en el repositorio digital de acceso abierto Zenodo.
Modelización cinética y cálculo dosimétrico
Se interpoló linealmente la captación (%ID/g) hasta 48 h a partir de los datos experimentales (4, 24 y 48 h) para todos los órganos. A partir de ese punto, para tumores, se consideró meseta hasta 96 h y descenso lineal hasta 168 h (7 días).
Para órganos no blanco, se extrapolaron los valores experimentales (4, 24 y 48 h) linealmente hasta 168 h; para tiroides se utilizó un descenso exponencial basado en estudios previos sobre captación tiroidea de radioyodo (9).
Las curvas tiempo-actividad fueron corregidas por decaimiento físico del ¹³¹I y el área bajo la curva fue integrada hasta siete días.
La dosis absorbida se estimó aplicando el formalismo/método del Comité de Dosis de Radiación Interna Médica (MIRD) para dosimetría interna (10) siguiendo metodologías utilizadas en estudios de radioinmunoterapia y radionúclidos terapéuticos (11).
Comparación
Se cotejaron los resultados con estudios de radioanticuerpos y radiofármacos dirigidos a tumores [131I-Tositumomab (4), 90Y-Ibritumomab (5), 177Lu-PSMA-617 (6)], todos integrados a 7 días.
RESULTADOS
Curvas de captación y dosimetría
Las curvas ajustadas mostraron una captación tumoral creciente hasta 48 h, meseta y posterior descenso en base a los datos experimentales hasta las 48h y la posterior extrapolación a 7 días, también se observa el efecto del decaimiento radioactivo (figura 1).
El pretratamiento con losartán aumentó la captación máxima y el área bajo la curva en tumor Tn+.
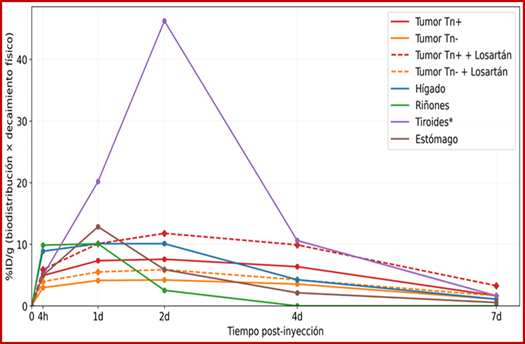
Figura 1. Cinética de captación de 131I-ChiTn (%ID/g) multiplicado por decaimiento radioactivo del 131I para todos los órganos. Los valores hasta 48 h corresponden a Tassano et al. 2024 (puntos experimentales), mientras que 4 y 7 días, extrapolación tomando los valores experimentales. * para tiroides se utilizó descenso exponencial según Lundh, et al. 2009 (9).
En la tabla 1 se resumen las dosis absorbidas calculadas en tumor para los distintos grupos analizados, incluyendo los tumores Tn+ y Tn- con y sin pretratamiento con losartán, y se comparan estos resultados con los valores reportados para otros anticuerpos y peptidos radiomarcados terapéuticos ampliamente utilizados.
Los resultados obtenidos muestran que la dosis absorbida en el tumor Tn+ tras el tratamiento con 131I-ChiTn es comparable a la lograda por anticuerpos aprobados para uso clínico, como 131I-tositumomab y 90Y-ibritumomab tiuxetan. Además, se observa que la administración de losartán incrementa la captación y la dosis especialmente en Tn+, destacando su potencial como adyuvante para mejorar la eficiencia de la radioinmunoterapia dirigida.
Tabla 1. Dosis absorbida en tumor (mGy/MBq, integración 0–7 días).
|
Radionucleido |
Anticuerpo / Target |
Grupo / Modelo |
Tumor (mGy/MBq) |
Bloqueo tiroideo |
Referencia |
|
131I |
ChiTn |
Tn+ sin losartán (ratón) |
1.5 (1.2–1.8) |
Sin |
Este trabajo / Tassano et al., 2024 (8) |
|
131I |
ChiTn |
Tn- sin losartán (ratón) |
0.8 (0.6–0.9) |
Sin |
Este trabajo / Tassano et al., 2024 (8) |
|
131I |
ChiTn |
Tn+ con losartán (ratón) |
1.8 (1.4–2.3) |
Sin |
Este trabajo / Tassano et al., 2024 (8) |
|
131I |
ChiTn |
Tn- con losartán (ratón) |
0.9 (0.7–1.1) |
Sin |
Este trabajo / Tassano et al., 2024 (8) |
|
131I |
Tositumomab (anti-CD20) |
Humano (linfoma, Bexxar) |
2.4 (2.0–3.0) |
Con |
Vose et al. 2000 (12) |
|
90Y |
Ibritumomab tiuxetan (CD20) |
Humano (linfoma, Zevalin) |
2.9 (2.1–4.3) |
N/A |
Witzig et al. 2002 (13) |
|
177Lu |
PSMA-617 (PSMA) |
Ratón (tumor prostático) |
2.2 (2.0–2.5) |
N/A |
Ray Banerjee et al. 2019 (14) |
En la tabla 2 se presenta la dosis absorbida estimada en los principales órganos no blanco (hígado, riñón, estómago y tiroides), permitiendo comparar la selectividad tumoral y el perfil de seguridad del radioanticuerpo 131I-ChiTn frente a otros anticuerpos y péptidos radiomarcados terapéuticos.
Se observa que las dosis en órganos no blanco se mantienen en rangos similares o inferiores a los descritos en la literatura para los anticuerpos clínicos de referencia.
Destaca el valor elevado observado en tiroides, explicado por la ausencia de bloqueo tiroideo en el modelo experimental, mientras que las dosis en hígado y riñón permanecen bajas, reflejando una favorable relación tumor/tejido sano.
Tabla 2. Dosis absorbida en órganos no blanco (mGy/MBq, integración 0–7 días)
|
Hígado |
Riñón |
Estómago |
Tiroides |
Bloqueo tiroideo |
Referencia |
|
|
131I-ChiTn, todos los grupos |
0.7 (0.6–0.7) |
0.6 (0–1.5) |
1.3 (1.0–1.6) |
4.4 (2.8–6.0) |
Sin |
Este trabajo / Tassano et al., 2024 (8) |
|
131I-Tositumomab (Bexxar, humano) |
0.7 (0.4–1.1) |
1.5 (0.8–2.0) |
0.5 (0.2–0.7) |
2–3 |
Con |
Vose et al. 2000 (12) |
|
90Y-Ibritumomab (Zevalin, humano) |
1.1 (0.8–1.6) |
0.6 (0.3–0.9) |
0.9 (0.6–1.2) |
<1 |
N/A |
Witzig et al. 2002 (13) |
|
177Lu-PSMA-617 (ratón) |
0.6 (0.5–0.7) |
0.5 (0.4–0.6) |
0.8 (0.7–1.0) |
– |
N/A |
Ray Banerjee et al. 2019 (14) |
DISCUSIÓN
El análisis dosimétrico realizado a partir de los datos experimentales publicados demuestra que la administración de ¹³¹I-ChiTn produce captación tumoral significativa en modelos murinos de tumor pulmonar Tn+.
El pretratamiento con losartán incrementó la captación tumoral y la dosis absorbida en tumores Tn+, lo que sugiere una mejora en la distribución intratumoral del radioanticuerpo.
Estos resultados son consistentes con estudios previos que han demostrado que la modulación farmacológica del microambiente tumoral puede mejorar la penetración de macromoléculas terapéuticas en tumores sólidos (3,5).
Los valores de dosis tumoral obtenidos se encuentran dentro del rango reportado para radioanticuerpos terapéuticos utilizados clínicamente, como ¹³¹I-tositumomab y ⁹⁰Y-ibritumomab tiuxetan (12,13).
Asimismo, las dosis estimadas en órganos no blanco fueron comparables a las reportadas en estudios previos con radioanticuerpos y péptidos radiomarcados (12-14).
La dosis elevada observada en tiroides puede atribuirse a la ausencia de bloqueo tiroideo en el modelo experimental, práctica que en humanos reduce significativamente la captación tiroidea de radioyodo (15).
Entre las limitaciones del estudio se incluyen la naturaleza preclínica del modelo y la simplificación de los modelos cinéticos utilizados para la extrapolación de las curvas tiempo-actividad.
No obstante, el enfoque dosimétrico utilizado es consistente con metodologías ampliamente aceptadas en radioinmunoterapia y medicina nuclear terapéutica (10,11).
CONCLUSIONES
Los datos experimentales reutilizados de Tassano et al., 2024, demuestran que 131I-ChiTn en modelos de tumor pulmonar Tn+ logra dosis tumorales comparables a radioanticuerpos clínicos.
El pretratamiento con losartán mejora la dosimetría tumoral sin aumentar la exposición a órganos no blanco.
La ausencia de bloqueo tiroideo elevó la dosis en tiroides; se recomienda su inclusión en futuros trabajos preclínicos.
DECLARACIÓN DE CONFLICTOS DE INTERESES
Los autores no reportan ningún conflicto de interés. El estudio se realizó con recursos propios de los autores y/o la institución a la que representan.
No uso de IA: los autores declaran que no se utilizó Inteligencia Artificial para la conceptualización o redacción de este artículo.
DECLARACIÓN ÉTICA
Todas las afirmaciones expresadas en este artículo son exclusivamente de los autores y no representan necesariamente las de sus organizaciones afiliadas, ni las del editor, ni los revisores. El editor no garantiza ni respalda ningún producto y/o afirmación que pueda evaluarse en este artículo.
REFERENCIAS
(1) Parakh S, Lee ST, Gan HK, Scott AM. Radiolabeled antibodies for cancer imaging and therapy. Cancers (Basel). 2022 Mar 11; 14(6):1454. https://doi.org/10.3390/cancers14061454 PMID: 35326605; PMCID: PMC8946248.
(2) Goldenberg DM. Targeted therapy of cancer with radiolabeled antibodies. J Nucl Med. 2002 May; 43(5):693-713. PMID: 11994535.
(3) Jain RK. Normalization of tumor vasculature: an emerging concept in antiangiogenic therapy. Science. 2005 Jan 7; 307(5706):58-62 https://doi.org/10.1126/science.1104819 PMID: 15637262.
(4) Jain M, Venkatraman G, Batra SK. Optimization of radioimmunotherapy of solid tumors: biological impediments and their modulation. Clin Cancer Res. 2007 Mar 1; 13(5):1374-82. https://doi.org/10.1158/1078-0432.CCR-06-2436 Epub 2007 Feb 19. PMID: 17309914.
(5) Chauhan VP, Martin J, Liu H, Lacorre D, Jain S, Kozin S, Stylianopoulos, T, Mousa A, Han X, Adstamongkonkul P, Popović Z, Huang P, Bawendi M, Boucher Y, Jain R. Angiotensin inhibition enhances drug delivery and potentiates chemotherapy by decompressing tumor blood vessels. Nat Commun. 2013; 4:2516. https://doi.org/10.1038/ncomms3516
(6) Munkley J. The role of sialyl-Tn in cancer. Int J Mol Sci. 2016 Feb 24; 17(3):275. https://doi.org/10.3390/ijms17030275 PMID: 26927062; PMCID: PMC4813139.
(7) Ando H, Matsushita T, Wakitani M, Sato T, Kodama-Nishida S, Shibata K, Shitara K, Ohta S. Mouse-human chimeric anti-Tn IgG1 induced anti-tumor activity against Jurkat cells in vitro and in vivo. Biol Pharm Bull. 2008 Sep; 31(9):1739-44. https://doi.org/10.1248/bpb.31.1739 PMID: 18758069.
(8) Tassano M, Camacho X, Freire T, Perroni C, da Costa V, Cabrera M, García MF, Fernandez M, Gambini JP, Cabral P, Osinaga E. Enhanced tumor targeting of radiolabeled mouse/human chimeric anti-Tn antibody in losartan-treated mice bearing Tn-expressing lung tumors. Cancer Biother Radiopharm. 2024 Jun; 39(5):337-348. https://doi.org/10.1089/cbr.2023.0138 Epub 2024 Jan 12. PMID: 38215243.
(9) Lundh C, Lindencrona U, Postgård P, Carlsson T, Nilsson M, Forssell-Aronsson E. Radiation-induced thyroid stunning: differential effects of 123I, 131I, 99mTc, and 211At on iodide transport and NIS mRNA expression in cultured thyroid cells. J Nucl Med. 2009; 50(7):1161–1167. https://doi.org/10.2967/jnumed.108.061150
(10) Loevinger R, Budinger TF, Watson EE. MIRD Primer for absorbed dose calculations. New York, NY: Society of Nuclear Medicine, 1991.
(11) Loke KS, Padhy AK, Ng DC, Goh AS, Divgi C. Dosimetric considerations in radioimmunotherapy and systemic radionuclide therapies: a review. World J Nucl Med. 2011 Jul; 10(2):122-38. https://doi.org/10.4103/1450-1147.89780 PMID: 22144871; PMCID: PMC3227338.
(12) Vose JM, Wahl RL, Saleh M, Rohatiner AZ, Knox SJ, Radford JA, Zelenetz AD, Tidmarsh GF, Stagg RJ, Kaminski MS. Multicenter phase II study of iodine-131 tositumomab for chemotherapy-relapsed/refractory low-grade and transformed low-grade B-cell non-Hodgkin's lymphomas. J Clin Oncol. 2000 Mar; 18(6):1316-23. https://doi.org/10.1200/JCO.2000.18.6.1316 PMID: 10715303.
(13) Witzig TE. Yttrium-90-ibritumomab tiuxetan radioimmunotherapy: a new treatment approach for B-cell non-Hodgkin's lymphoma. Drugs of Today (Barcelona, Spain: 1998). 2004 Feb; 40(2):111-119. https://doi.org/10.1358/dot.2004.40.2.799423 PMID: 15045033.
(14) Ray Banerjee S, Kumar V, Lisok A, Chen J, Minn I, Brummet M, Boinapally S, Cole M, Ngen E, Wharram B, Brayton C, Hobbs R, Pomper M. 177Lu-labeled low-molecular-weight agents for PSMA-targeted radiopharmaceutical therapy. Eur J Nucl Med Mol Imaging. 2019 November; 46(12): 2545–2557. https://doi.org/10.1007/s00259-019-04434-0
(15) Behr TM, Juweid ME, Sharkey RM, Dunn RM, Ying Z, Becker WS, Siegel JA, Goldenberg DM. Thyroid radiation doses during radioimmunotherapy of CEA-expressing tumours with 131I-labelled monoclonal antibodies. Nucl Med Commun. 1996 Sep; 17(9):767-80. https://doi.org/10.1097/00006231-199609000-00007 PMID: 8895904. 1996.
NOTA: los datos de investigación se encuentran disponibles en Zenodo. Datos abiertos: https://zenodo.org/records/8110446
CONTRIBUCIONES AL MANUSCRITO:
(a) Concepción, adquisición y análisis de datos, interpretación y discusión de resultados, redacción y aprobación de la versión final.
(b) Diseño, adquisición y análisis de datos, interpretación y discusión de resultados, redacción.
Recibido para evaluación: diciembre 2025.
Aceptado para publicación: febrero 2026.
Fecha de publicación: marzo 2026.
Correspondencia: Facultad de Ciencias. Iguá 4225. C.P. 11400. Tel.: (+598) 2525 8618. Montevideo, Uruguay.
E-mail de contacto: marcos.tassano@fcien.edu.uy
![]() Salud Mil 2026; 45(1):1-10. https://doi.org/10.35954/SM2026.45.1.2.e301 e-ISSN 1688-0633.
Salud Mil 2026; 45(1):1-10. https://doi.org/10.35954/SM2026.45.1.2.e301 e-ISSN 1688-0633.